비회원이 작성한 글입니다!
글작성시 입력했던 비밀번호를 입력해주세요.
| ApoE4→ApoE3 바꾸는 저분자화합물 발굴.. | |
|---|---|
| 관리자 조회수 1313 | 2018/04/13 |
|
Gladstone Institutes 연구팀, 저분자화합물 PH002로 ApoE4 →ApoE3-유사 구조로 바꿔 "실제 병리작용 회복 확인"...쥐에서 ApoE4 병리작용 일으키지 않아, 기존 AD 동물모델에 의문제기 ▲Nature Medicine에 9일자로 'Gain of toxic apolipoprotein E4 effects in human iPSC-derived neurons is ameliorated by a small-molecule structure corrector'라는 제목으로 게재된 논문. doi: 10.1038/s41591-018-0004-z
알츠하이머병을 치료할 수 있는 타깃으로 ApoE4가 조명받고 있다. Gladstone Institutes 연구팀은 알츠하이머병을 발병하는 ApoE4(Apolipoprotein E4)를 ApoE3로 바꿀 수 있는 약물을 발굴했다. 연구팀은 이 약물을 통해 ApoE4를 ApoE3-유사(like) 형태로 바꾸는데 성공했으며, 이에 따라 알츠하이머병의 병리증상이 회복되는 것을 확인했다. 또한 연구팀은 인간 뉴런(neuron)에서 ApoE4 변이가 알츠하이머병 병리기전에 영향을 끼치는 것과는 달리 쥐에서는 이같은 현상이 일어나지 않음을 밝혔다. 이제까지 전임상 실험에서 사용되는 ApoE4 유전자변이 동물모델에 의문을 제기하는 결과로 학계, 산업계에 큰 반향을 불러일으키고 있다. 연구팀은 지난 9일 Nature Medicine에 'Gain of toxic apolipoprotein E4 effects in human iPSC-derived neurons is ameliorated by a small-molecule structure corrector'라는 제목의 논문을 게재했다. 정상상태인 ApoE3(Apolipoprotein E3)에 유전자변이가 발생해 ApoE3의 122번 아미노산 잔기가 시스테인(Cys)에서 아르지닌(Arg)으로 바뀌면서 ApoE4가 된다. 이로인해 기능이 망가지고 뉴런은 변형된 ApoE4 절편을 세포밖으로 분비해 뇌에 손상을 일으키게 된다. ApoE3 보유자와 비교했을때 ApoE4 유전자를 1개(copy) 보유할 경우 알츠하이머병 발병률이 2배, ApoE4 유전자를 2개 가질경우 12배 높아진다고 알려져 있다. ApoE4가 알츠하이머병 발병인자로 꼽히는 이유다. 그러나 아직까지 인간 뉴런에서 ApoE4에 따른 병리기전은 알려지지 않았다. 이에 연구팀은 최초로 ApoE4 변이를 가진 인간 역분화줄기세포(iPSC, induced Pluripotent stem cells)를 이용해 ApoE4가 알츠하이머병 발병률을 높이는 원인기전을 추적했다. 인간 뉴런에서 ApoE4 절편...p-타우, 아밀로이드 생성, GABAergic 뉴런퇴행↑ 연구팀은 대조군(ApoE3-발현 뉴런)과 비교했을떄 ApoE4/4-발현 뉴런에서 인산화타우(p-Tau, tau phosphorylation)를 높게 발현하며(p<0.0001), 두가지 베타 아밀로이드인 Aβ40, Aβ42를 두배 이상 발현한다는 것을 관찰했다. 단 p-타우와 아밀로이드의 생성에는 연관성이 없었다. 이밖에도 억제성 신호전달 신경세포인 GABAergic 뉴런의 신경퇴행이 나타났다. 모두 기존에 알츠하이머병의 주요 병리기전으로 알려진 요소다. 다음으로 연구진은 ApoE3의 기능이 감소하는 것이 문제를 일으키는지, 혹은 ApoE4 자체가 독성인자로 작용하는지를 규명하기 위해 유전자편집(gene editing) 기술을 이용해 실험을 진행했다. 그결과 ApoE가 없는 신경세포는 ApoE3와 똑같이 기능했지만, ApoE4가 존재할 경우 알츠하이머병의 병리적 특성이 나타나는 것을 확인했다. 즉 치료제의 개발뱡항은 독성인자인 ApoE4를 제거하는 데 있다는 것을 의미하는 결과다.
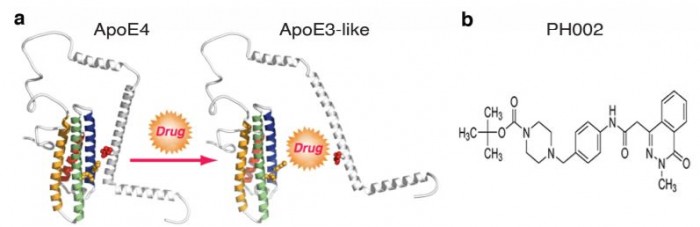 ▲논문 Supplement data, 약물의 작용기전 및 구조
흥미롭게도 연구팀은 ApoE4의 구조를 변형해 병리작용을 일으키지 않는 ApoE3-유사구조를 만드는 저분자화합물인 'PH002'를 발굴했다. 실제 ApoE4/4-발현 iPSC에 테스트했을 때 약물 용량의존적으로 ApoE4 절편이 유의미하게 감소하고, GABAergic 뉴런이 증가한 것을 관찰했다. p-타우, 아밀로이드의 수준 또한 감소했다. ApoE4 뉴런에서 보인 주요 병리증상이 회복된 것이다. ApoE4를 타깃하는 저분자화합물 신약개발의 가능성을 보여주는 데이터다. 어쩌면 쥐에서 효과가 있었던 약물이, 임상서 실패했던 이유? 인간 뉴런에서 ApoE4의 병리기전을 밝히고, 이를 타깃하는 저분자화합물을 찾은 것 외에도 이번 논문이 주목받는 이유는 또 있다. 쥐 뉴런에서 ApoE4의 존재에 따라 아밀로이드 생산에 변화가 없었기 때문이다. 종에 따라 ApoE4의 대사 및 작용기전이 다르다는 것을 보여주는 결과다. ApoE4 모델쥐 등 전임상에서 성공했던 신약 후보물질이 임상에서 실패했던 이유였다는 해석이다. 이번 결과는 알츠하이머병 신약개발에도 큰 영향을 미칠 것으로 해석된다. 논문 저자인 Chengzhong Wang는 "apoE4가 아밀로이드 베타에 미치는 영향에는 종간차이가 있다"며 "동물실험에서 유망한 결과를 보였던 신약 후보물질이 임상에서 실패했는지에 대한 단서를 제공할 뿐만 아니라 인간 모델 시스템에서 알츠하이머병 연구를 해야된다는 것을 보여주는 결과"라고 강조했다. 덧붙여 연구진은 "이번 결과는 ApoE4 구조를 바꾸는 약물개발을 뒷받침한다"며 "궁극적으로 임상에 돌입할 것"이라고 밝혔다. 한편, 최근 ApoE4를 치료타깃으로 겨냥하는 시도가 늘어나고 있다. 지난달 미국 워싱턴대학교 의과대학 연구진은 뇌의 ApoE4만 특이적으로 타깃하는 항체인 'HAE-4'가 아밀로이드를 제거하는 작용이 있음을 증명했다. 항체의 Fcγ 수용체 작용을 통해 미세아교세포(microglia)가 아밀로이드를 제거하는 기전이다. 또한 연구팀은 APOE 항체는 플라크의 작은 부분만 타깃하기 때문에, 기존의 아밀로이드 항체와 비교해 적은 면역활성을 보여 원치않은 부작용이 적을 것으로 예측했다. 해당 항체는 미국 뇌질환 치료제개발 전문기업인 디날리테라퓨틱스(Denali therapeutics)가 라이선스해 개발할 계획이다. 바이오스펙테이터 김성민 기자 sungmin.kim@bios.co.kr |
|


